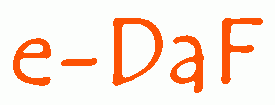 |
Chemie:
Periodensystem
der
Elemente
- Übungsaufgabe  Mit dem Mauszeiger können Sie die Eigenschaften der Elemente anzeigen. |

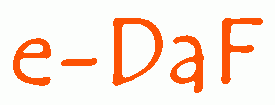 |
Chemie:
Periodensystem
der
Elemente
- Übungsaufgabe  Mit dem Mauszeiger können Sie die Eigenschaften der Elemente anzeigen. |
